
Presentación de Caso
Metastasectomía hepática secuencial en cáncer colorrectal oligometastásico
Sequential Hepatic Metastasectomy in Oligometastatic Colorectal Cancer
Roberto Lázaro Blanco-Sosa1* https://orcid.org/0000-0001-9475-9517
Oscar Israel Delgado Rodriguez2 https://orcid.org/0009-0009-9172-8008
Carlos David García Martín3 https://orcid.org/0009-0002-3273-4247
Milton Manuel Sánchez García4 https://orcid.org/0000-0002-7333-9107
1Especialista de Primer Grado en Cirugía General. Alta Especialidad en Cirugía Hepatopancreatobiliar. Master en Trasplante Hepático. Servicio de Cirugía Hepatopancreatobiliar. Instituto Nacional de Ciencias Médicas y Nutrición Salvador Zubirán. Ciudad de México, México.
2Facultad de Medicina. Universidad Autónoma de San Luis Potosí. San Luis Potosí, México.
3Médico residente en Cirugía General. Universidad Mariano Gálvez de Guatemala. Servicio de Cirugía General. Hospital Regional de Huehuetenango. Huehuetenango, Guatemala.
4Especialista de Primer Grado en Cirugía General. Instructor. Servicio de Cirugía Hepatobiliopancreatica. Hospital Clínico Quirúrgico Hermanos Ameijeiras. La Habana, Cuba.
*Autor para correspondencia: roberto.blancos@incmnsz.mx

RESUMEN
Introducción:
El cáncer colorrectal es una de las principales causas de mortalidad
por cáncer a nivel mundial. Aunque una proporción significativa
de pacientes debuta con enfermedad metastásica, el concepto de enfermedad
oligometastásica ha permitido identificar un subgrupo susceptible de
tratamiento con intención curativa mediante estrategias multimodales.
Objetivo:
Describir los aspectos clínicos, quirúrgicos y moleculares
de un paciente con adenocarcinoma de colon sigmoides con metástasis hepáticas
oligometastásicas.
Presentación
del caso: Se describe el caso de un paciente masculino de 55 años
con adenocarcinoma de colon sigmoides que se presentó con rectorragia.
La estadificación inicial evidenció metástasis hepáticas
oligometastásicas sin enfermedad extrahepática. El estudio molecular
mostró estatus pMMR y mutación de KRAS p.G12A. El paciente recibió
quimioterapia perioperatoria con capecitabina y oxaliplatino, logrando una respuesta
parcial significativa. Posteriormente, se realizó una estrategia quirúrgica
en dos tiempos que incluyó metastasectomía hepática con
ablación complementaria y, en un segundo tiempo, resección laparoscópica
del tumor primario. El análisis histopatológico confirmó
adenocarcinoma moderadamente diferenciado sin compromiso ganglionar y un margen
vascular positivo en la resección hepática. La evolución
clínica fue favorable, con adecuada tolerancia al tratamiento adyuvante,
normalización del antígeno carcinoembrionario y ausencia de progresión
en el seguimiento temprano.
Conclusión:
En pacientes cuidadosamente seleccionados, el tratamiento multimodal puede ofrecer
resultados oncológicos alentadores en el cáncer colorrectal oligometastásico
hepático.
Palabras clave: Neoplasias colorrectales; Metástasis hepáticas; Enfermedad oligometastásica; Hepatectomía.
ABSTRACT
Introduction:Colorectal
cancer is one of the leading causes of cancer-related mortality worldwide. Although
a significant proportion of patients present with metastatic disease at diagnosis,
the concept of oligometastatic disease has enabled the identification of a subgroupp
otentially amenable to curative-intent treatment through multimodal strategies.
Objetive:
To describe the clinical, surgical and molecular aspects of a patient with
sigmoid colon adenocarcinoma with oligometastatic liver metastases.
Case presentation:
We report the case of a 55-year-old male patient with sigmoid colon adenocarcinoma
whop resented with rectal bleeding. Initial staging revealed oligometastatic
liver disease without extra hepatic involvement. Molecular analysis demonstrated
proficient mismatch repair (pMMR) status and a KRAS p.G12A mutation. The patient
received perioperative chemotherapy with capecitabine and oxaliplatin, achieving
a significant partial response. Subsequently, a two-stage surgical strategy
was performed, including hepatic metastasectomy with complementary ablation,
followed by laparoscopic resection of the primary tumor. Histopathological analysis
confirmed a moderately differentiated adenocarcinoma without lymphnode involvement
and a positive vascular margin in thehepaticresection. The clinical course was
favorable, with good tolerance to adjuvant therapy, normalization of carcinoembryonic
antigen levels, and no evidence of disease progression during early follow-up.
Discussion:
This case highlights the value of a multidisciplinary approach in patients with
oligometastatic colorectal cancer totheliver, emphasizing the role of perioperative
chemotherapy as a tool for biological selection and the feasibilityof a two-stage
surgical approach even in thepresence of adverse prognostic factors.
Conclusion:
In carefully selected patients, multimodal treatment may provide encouraging
oncological outcomes in oligometastati ccolorectal liver metastases.
Keywords: Colorectal Neoplasms; Liver Metastases; Oligometastatic Disease; Hepatectomy.
Recibido: 21/02/2026
Aprobado: 21/04/2026
INTRODUCCIÓN
El cáncer colorrectal (CCR) representa una de las principales causas de morbilidad y mortalidad por cáncer a nivel mundial(1). Alrededor del 20 y 25 % de los pacientes presentan enfermedad metastásica al momento del diagnóstico, siendo el hígado el sitio más frecuente de diseminación(2). En este contexto, las metástasis hepáticas de origen colorrectal constituyen un escenario clínico complejo, en el que el abordaje multidisciplinario es fundamental para optimizar los resultados oncológicos.(3)
En los últimos años, el concepto de enfermedad oligometastásica ha cobrado especial relevancia, al describir un subgrupo de pacientes con carga metastásica limitada, con gran susceptibilidad de tratamientos con intención curativa(4). En estos casos, la combinación de quimioterapia sistémica perioperatoria y resección quirúrgica de las metástasis hepáticas, ha demostrado mejorar la supervivencia global y libre de enfermedad, en especial cuando se logra una adecuada selección de pacientes.(5)
El desarrollo de terapias sistémicas más eficaces, junto con avances en las técnicas quirúrgicas hepáticas y la estratificación molecular del CCR, ha permitido ampliar las indicaciones de resección hepática, incluso en escenarios considerados al inicio como irresecables.(6) No obstante, persisten controversias respecto al momento óptimo de la cirugía, la secuencia terapéutica ideal y el impacto pronóstico de factores como el estatus molecular, los márgenes quirúrgicos y la respuesta al tratamiento sistémico.(7)
En este contexto, presentamos el caso de un paciente con adenocarcinoma de colon sigmoides con metástasis hepáticas oligometastásicas, tratado mediante una estrategia perioperatoria con quimioterapia basada en oxaliplatino y cirugía en dos tiempos. El objetivo de este trabajo es describir los aspectos clínicos, quirúrgicos y moleculares de un paciente con adenocarcinoma de colon sigmoides con metástasis hepáticas oligometastásicas.
PRESENTACIÓN DEL CASO
Paciente masculino de 55 años, con antecedentes personales de dislipidemia mixta, prediabetes y enfermedad hemorroidal grado I. Presentaba antecedente de tabaquismo significativo (31 paquetes-año), suspendido a los 47 años, así como consumo ocasional de alcohol. Negaba antecedentes quirúrgicos relevantes. Dentro de los antecedentes heredofamiliares destacaba una fuerte carga oncológica, con cáncer de páncreas en el abuelo paterno, cáncer de próstata con metástasis óseas en el padre, cáncer de pulmón y páncreas en un tío paterno, y cáncer de tejidos blandos de localización pélvica en una tía paterna.
El paciente inició su padecimiento actual en marzo de 2025, caracterizado por episodios de rectorragia y hematoquecia, sin pérdida ponderal significativa ni síntomas constitucionales asociados. Como parte del abordaje diagnóstico, se realizó colonoscopía el 31 de marzo de 2025, la cual evidenció una lesión tumoral en colon sigmoides, localizada a 15 cm del margen anal. La biopsia endoscópica confirmó el diagnóstico de adenocarcinoma moderadamente diferenciado.
Para estadificación inicial, se efectuó un estudio PET/CT con ^18F-FDG el 4 de abril de 2025, el cual mostró una lesión hipermetabólica en colon sigmoides de aproximadamente 5,5 cm, con infiltración transmural, así como múltiples lesiones hepáticas hipermetabólicas compatibles con metástasis, localizadas en el segmento VI (dos lesiones de 51 × 38 mm y 18 × 15 mm) y en el segmento II (una lesión de 12 mm). No se identificaron metástasis extrahepáticas ni adenopatías a distancia. El nivel sérico de antígeno carcinoembrionario (CEA) al momento del diagnóstico fue de 13,7 ng/mL.
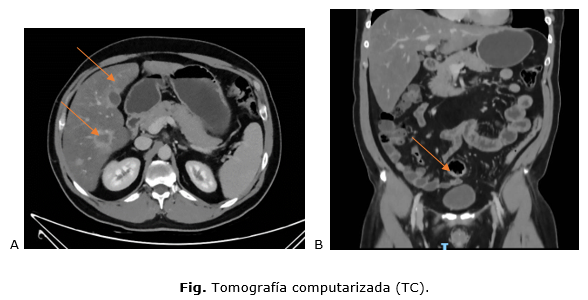
A. Corte axial
de TC
Imagen axial de abdomen que muestra lesiones hepáticas metastásicas
en el segmento VI (51 × 38 mm y 18 × 15 mm) y segmento II (12 mm),
hipodensas y bien delimitadas. No se identifican adenopatías a distancia
ni otras lesiones extrahepáticas.
B. Corte sagital
de TC
Imagen sagital de abdomen evidenciando la localización del adenocarcinoma
de colon sigmoides y su relación con el hígado. Se aprecian las
metástasis oligometastásicas y el compromiso transmural del colon,
así como la anatomía hepática previa a la resección
quirúrgica.
El análisis molecular del tumor primario reveló un estatus de reparación de errores de apareamiento del ADN competente (pMMR), con conservación de la expresión de MLH1, MSH2, MSH6 y PMS2, mutación de KRAS p.G12A en el exón 2 y negatividad para HER2. Con base en estos hallazgos, el caso se clasificó como adenocarcinoma de colon sigmoides estadio IV con enfermedad hepática oligometastásica.
Se decidió iniciar tratamiento sistémico perioperatorio con quimioterapia basada en capecitabina y oxaliplatino (CAPOX). El paciente completó cuatro ciclos entre abril y junio de 2025, para lo cual presentó adecuada tolerancia, con toxicidad limitada a náusea grado 1 y neuropatía sensitiva periférica grado 1, sin necesidad de ajustes de dosis.
La evaluación de respuesta mediante tomografía computarizada de tórax, abdomen y pelvis realizada el 1 de julio de 2025 mostró una respuesta parcial conforme a los criterios RECIST 1.1, con una reducción aproximada del 41 % del volumen de las metástasis hepáticas, así como resolución de adenopatías regionales previamente descritas, sin evidencia de nuevas lesiones.
Tras la evaluación por un equipo multidisciplinario, se decidió una estrategia quirúrgica en dos tiempos. El 28 de julio de 2025, el paciente fue sometido a cirugía hepática, se le realizó metastasectomía del segmento VI y ablación de la lesión del segmento II. Durante el procedimiento se realizaron dos maniobras de Pringle, de 15 y 24 minutos respectivamente. El posoperatorio inmediato cursó sin complicaciones mayores, se observó solo hiperlactatemia transitoria que se resolvió con manejo conservador. El estudio histopatológico de las piezas hepáticas demostró adenocarcinoma metastásico de tipo mucinoso con extensa necrosis tumoral, con un tamaño máximo de 1,6 × 3 cm y margen vascular positivo.
Luego, el 23 de septiembre de 2025, se efectuó sigmoidectomía laparoscópica con anastomosis colorrectal primaria. El análisis histopatológico reveló un adenocarcinoma moderadamente diferenciado de 3 × 2,7 cm, con invasión a través de la muscular propia hasta la serosa (pT3), ausencia de invasión linfovascular, presencia de invasión perineural, márgenes quirúrgicos negativos y ausencia de metástasis ganglionares (0 de 3 ganglios examinados). El estadio patológico final fue pT3 pN0 pM1a.
En el seguimiento postoperatorio, una tomografía de control realizada en octubre de 2025 mostró cambios postquirúrgicos esperados, sin evidencia de enfermedad metastásica activa. Algunas alteraciones hepáticas mal definidas fueron interpretadas como cambios postratamiento y se dejaron en vigilancia estrecha. El paciente inició tratamiento adyuvante con CAPOX en octubre de 2025.
Al último seguimiento, en diciembre de 2025, el paciente se encontraba asintomático, con estado funcional ECOG 0, adecuada tolerancia al tratamiento sistémico, normalización de los niveles de CEA y sin evidencia clínica ni radiológica de progresión de la enfermedad.
DISCUSIÓN
La enfermedad hepática metastásica de origen colorrectal continúa siendo uno de los principales determinantes pronósticos en pacientes con CCR avanzado.(8) Sin embargo, un subgrupo bien definido de pacientes con enfermedad oligometastásica puede beneficiarse de un enfoque terapéutico agresivo y multimodal, con intención curativa.(4,9) El caso presentado ilustra de manera clara este escenario y resalta varios aspectos de interés clínico y académico.
En primer lugar, la adecuada estadificación inicial fue clave para la toma de decisiones terapéuticas. El uso de PET/CT permitió confirmar la localización exclusiva de la enfermedad metastásica al hígado y descartar compromiso extrahepático, lo cual es un requisito fundamental para considerar estrategias quirúrgicas con intención curativa(10). Asimismo, la elevación moderada del CEA al diagnóstico y su posterior normalización tras el tratamiento sistémico constituyeron marcadores indirectos de respuesta tumoral.(11)
El tratamiento sistémico perioperatorio con CAPOX desempeñó un papel central en el manejo de este paciente. La quimioterapia neoadyuvante permitió reducir de forma significativa el tamaño de las metástasis hepáticas, lo que facilita su abordaje quirúrgico y sirve además como prueba de sensibilidad tumoral.(5,12) La respuesta parcial observada, conforme a criterios RECIST, se ha asociado en múltiples estudios con mejores desenlaces oncológicos, al reflejar un comportamiento biológico más favorable.(13)
La decisión de realizar una estrategia quirúrgica en dos tiempos respondió a la necesidad de un control óptimo tanto de la enfermedad hepática como del tumor primario, lo cual minimiza el riesgo de complicaciones y permite una adecuada recuperación entre procedimientos.(14) Este enfoque escalonado es aceptado en pacientes seleccionados con metástasis hepáticas resecables o potencialmente resecables, y ha demostrado ser seguro y eficaz cuando se realiza en centros con experiencia.
Un hallazgo relevante en este caso fue la presencia de un margen vascular positivo en la resección hepática. Si bien los márgenes positivos se han asociado con peor pronóstico, evidencia reciente sugiere que, en el contexto de una adecuada respuesta a la quimioterapia y ausencia de enfermedad macroscópica residual, su impacto puede ser mitigado.(14) El seguimiento estrecho y la administración de tratamiento adyuvante resultan fundamentales en estos escenarios.
Desde el punto de vista patológico y molecular, la identificación de un adenocarcinoma moderadamente diferenciado, con invasión perineural pero sin compromiso ganglionar, junto con un estatus pMMR y mutación de KRAS p.G12A, aporta información pronóstica y terapéutica relevante. La mutación de KRAS, si bien limita el uso de terapias anti-EGFR, no contraindica un enfoque quirúrgico agresivo en pacientes con enfermedad oligometastásica y adecuada respuesta al tratamiento sistémico.(14)
La evolución clínica favorable del paciente, con adecuado estado funcional, normalización de marcadores tumorales y ausencia de progresión radiológica en el seguimiento temprano, refuerza la importancia del manejo multidisciplinario en el CCR metastásico. Este caso subraya que, en pacientes seleccionados con cuidado, la combinación de quimioterapia perioperatoria y cirugía puede ofrecer resultados alentadores incluso en estadios avanzados de la enfermedad.
CONCLUSIÓN
El presente caso ilustra la importancia del abordaje multidisciplinario en pacientes con cáncer colorrectal metastásico limitado al hígado. En un contexto de enfermedad oligometastásica, la combinación de quimioterapia sistémica perioperatoria y cirugía en dos tiempos permitió un adecuado control oncológico, con respuesta tumoral significativa, resección del tumor primario y manejo dirigido de las metástasis hepáticas. A pesar de la presencia de factores pronósticos desfavorables, como la mutación de KRAS y un margen vascular positivo en la resección hepática, la evolución clínica favorable del paciente resalta que estos hallazgos no contraindican una estrategia con intención curativa en pacientes seleccionados con cuidado. Este caso refuerza el papel de la quimioterapia como herramienta de selección biológica y subraya la necesidad de individualizar el tratamiento en el cáncer colorrectal metastásico, en particular en aquellos escenarios de enfermedad oligometastásica.
REFERENCIAS BIBLIOGRAFICAS
1. Sung H, Ferlay J, Siegel RL. Global cancerstatistics 2020. CA Cancer J Clin. 2021;71:209-249. [acceso 12/01/2026]. Disponible en: https://acsjournals.onlinelibrary.wiley.com/doi/10.3322/caac.21660
2. Van Cutsem E, Cervantes A, Nordlinger B, Arnold D. Metastaticcolorectalcancer: ESMO Clinical Practice Guidelines. Ann Oncol. 2014;25(Suppl 3):iii1-iii9. [acceso 19/01/2026]. Disponible en: https://www.annalsofoncology.org/article/S0923-7534(19)36408-2/fulltext
3. Adam R, de Gramont A, Figueras J. Managing synchronous liver metastases from colorectal cancer. Ann Surg. 2015;261:103-114. [acceso 03/02/2026]. Disponible en: https://journals.lww.com/annalsofsurgery/Fulltext/2015/01000/Managing_Synchronous_Liver_Metastases_from.19.aspx
4. Hellman S, Weichselbaum RR. Oligometastases. J Clin Oncol. 1995;13:8-10. [acceso 25/01/2026]. Disponible en: https://ascopubs.org/doi/10.1200/JCO.1995.13.1.8
5. Nordlinger B, Sorbye H, Glimelius B. Perioperative chemotherapy with FOLFOX4 and surgery versus surgery alone. Lancet. 2008;371:1007-1016. [acceso 17/01/2026]. Disponible en: https://www.thelancet.com/journals/lancet/article/PIIS0140-6736(08)60305-6/fulltext
6. Adam R, Wicherts DA, de Haas RJ. Patients with initially unresectable colorectal liver metastases. J Clin Oncol. 2009;27:1829-1835. [acceso 30/01/2026]. Disponible en: https://ascopubs.org/doi/10.1200/JCO.2008.20.1195
7. de Jong MC, Pulitano C, Ribero D. Rates and patterns of recurrence following curative intentsurgery. Ann Surg. 2009;250:440-448. [acceso 09/02/2026]. Disponible en: https://journals.lww.com/annalsofsurgery/Fulltext/2009/09000/Rates_and_Patterns_of_Recurrence_Following.3.aspx
8. Choti MA, Sitzmann JV, Tiburi MF. Trends in long-term survivalf ollowing liver resection. Ann Surg. 2002;235:759-766. [acceso 22/01/2026]. Disponible en: https://journals.lww.com/annalsofsurgery/Fulltext/2002/06000/Trends_in_Long_Term_Survival_Following_Liver.15.aspx
9. Ruers T, Van Coevorden F, Punt CJA. Local treatment of unresectable colorectal liver metastases. Lancet Oncol. 2017;18:e61-e69. [acceso 05/02/2026]. Disponible en: https://www.thelancet.com/journals/lanonc/article/PIIS1470-2045(16)30586-6/fulltext
10. Ruers TJ, Wiering B, van derSijp JR. Improved selection of patients for hepatic surgery using PET. J Clin Oncol. 2009;27:439-446. [acceso 14/01/2026]. Disponible en: https://ascopubs.org/doi/10.1200/JCO.2008.19.8534
11. Okuno K, Ueno M, Murata K. Prognostic significance of CEA normalization. Dis Colon Rectum. 1999;42:1558-1564. [acceso 28/01/2026]. Disponible en: https://journals.lww.com/dcrjournal/Fulltext/1999/11000/Prognostic_Significance_of_CEA_Normalization.15.aspx
12. Adam R, Pascal G, Castaing Dl. Tumor progression while on chemotherapy. J Clin Oncol. 2004;22:2068-2074. [acceso 08/02/2026]. Disponible en: https://ascopubs.org/doi/10.1200/JCO.2004.07.043
13. Eisenhauer EA, Therasse P, Bogaerts J. New response evaluation criteria in solidt umours (RECIST 1.1). Eur J Cancer. 2009;45:228-247. [acceso 16/01/2026]. Disponible en: https://www.sciencedirect.com/science/article/pii/S0959804908007123
14. Karagkounis G, Torbenson MS, Daniel HD. KRAS mutation and outcomes after liver resection. Ann Surg Oncol. 2013;20:4137-4144. [acceso 26/01/2026]. Disponible en: https://link.springer.com/article/10.1245/s10434-013-3045-6
Conflicto de intereses
Los autores declaran que no hay conflictos de intereses.
Financiación
Los autores declaran que no recibieron financiación para el desarrollo del presente artículo.
Contribuciones de los autores
Conceptualización:
Roberto Lázaro Blanco-Sosa, Oscar Israel Delgado Rodriguez, Carlos David
García Martín, Milton Manuel Sánchez García.
Curación
de datos: Roberto Lázaro Blanco-Sosa, Carlos David García Martín.
Análisis
Formal: Roberto Lázaro Blanco-Sosa.
Adquisición
de financiamiento: Carlos David García Martín, Oscar Israel Delgado
Rodriguez, Milton Manuel Sánchez García.
Investigación:
Roberto Lázaro Blanco-Sosa, Oscar Israel Delgado Rodriguez,Carlos David
García Martín, Milton Manuel Sánchez García.
Metodología:
Carlos David García Martín, Oscar Israel Delgado Rodriguez, Milton
Manuel Sánchez García.
Administración
del Proyecto: Oscar Israel Delgado Rodriguez,Carlos David García Martín,
Milton Manuel Sánchez García.
Recursos:
Carlos David García Martín.
Software:
Carlos David García Martín, Oscar Israel Delgado Rodriguez.
Supervisión:
Roberto Lázaro Blanco-Sosa.
Validación:
Roberto Lázaro Blanco-Sosa.
Visualización:
Carlos David García Martín.
Redacción
- Elaboración del borrador original: Roberto Lázaro Blanco-Sosa.
Redacción
- Revisión y edición: Roberto Lázaro Blanco-Sosa, Carlos
David García Martín, Milton Manuel Sánchez García,
Oscar Israel Delgado Rodriguez.